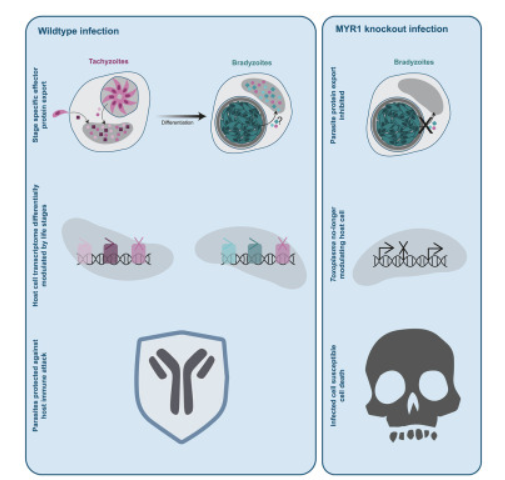
Tonkin说,潜伏性感染是全球最大的健康负担之一。他说,“艾滋病、肝炎、疟疾和肺结核等疾病都是慢性或潜伏性感染的例子,它们造成了重大疾病、残疾和经济影响。如果我们能够了解是什么导致这些潜伏感染重新激活,以及它们对我们的细胞和大脑的控制,我们将走上寻找新的治疗方法的道路,以减轻一些最贫困的人的负担。”
T细胞
Aifantis说,“我们的临床方法将涉及使用低缬氨酸饮食,将急性淋巴细胞白血病中的T细胞数量缩减到如此低的水平,以至于药物可以有效地阻滞癌症进展。”
Aifantis说,许多基本的细胞组分,包括蛋白、核苷酸和脂肪酸,都是癌症生长和扩散所需要的。至少有6种其他的氨基酸,特别是高水平的赖氨酸,与癌症有关,但是它们的确切作用仍然未知。他提醒说,几十年来,人们一直在尝试单纯的饮食策略来治疗癌症,但几乎没有科学证据表明有任何好处。他说,在推荐任何治疗方案之前,还需要开展更多的研究,包括这些作者计划的临床试验。
美国癌症协会估计,每年有超过1500名美国人死于T细胞急性淋巴细胞白血病,其中大部分是儿童。另有5000人将被新诊断出来。这种类型的癌症大约占所有白血病的四分之一。
这些作者计划在明年测试低缬氨酸含量的饮食,如肉类、鱼类和豆类,是否是针对癌症患者的有效治疗方法。Thandapani说,低缬氨酸饮食很容易获得,因为它们已经被用于治疗与影响肠道代谢的遗传性疾病有关的体内酸失衡。
论文共同通讯作者、纽约大学朗格尼健康中心的Iannis Aifantis博士说,临床试验设计可能会将饮食疗法与维奈托克(venetoclax)相结合,维奈托克是一种已经在美国被批准用于治疗大多数其他类型白血病的药物。
他说,药物组合很重要,因为这种饮食限制不可能长期持续。这是由于已知的长期缬氨酸缺乏可能导致肌肉萎缩和脑损伤。
在保持分化能力和表观遗传学完整性的同时,分离具有原始多能性特征的人类MEK/ERK信号无关的多能干细胞(PSCs)仍然具有一定的挑战性;实现培养的器官用于挽救生命的移植程序的愿景仍然是一个漫长的过程,然而,来自以色列魏茨曼科学研究所等机构的科学家们在干细胞方面的工作正在为这一目标的实现铺平了道路,相关研究结果以题为“Principles of signaling pathway modulation for enhancing human naive pluripotency induction”的报告刊登在了国际杂志Cell Stem Cell上。
文章中,研究人员开发出了一种新方法,其可以在比以前更早的状态下培养人类干细胞,不仅如此,研究人员所创造的干细胞或许还具有更强的能力,这意味着其能有效地与宿主环境融合,这或许就大大提高了获得所谓的跨物种嵌合体的机会,即允许一种生物体的细胞在另一种生物的发育中发挥重要作用。最近的研究结果表明,由于人类细胞处于未分化的状态,其能发育成为体内任何类型的细胞,包括其它干细胞,因此研究者就能制造出非常早期的人类细胞并成功将其融入小鼠机体内;此外研究人员还提出了一种步骤来显著提高这些细胞整合的能力,而提高研究者创造并研究这些细胞类型的能力,未来或能用于将细胞从一种动物转移到另一种动物体内,比如人类机体中。
早在2013年研究人员就取得了突破性的进展,他们率先将人类干细胞注射到小鼠体内并发现注射的干细胞或能成功整合到小鼠发育中的胚胎中,这项研究成果首次发表8年后,研究人员进一步尝试产生更早期完全原始的干细胞用于类似的程序;当他们认为这一想法几乎不可能实现的时候,研究者表示,我们在小鼠机体中所产生类似细胞的经验告诉我们,这一过程或许困难重重。这些细胞通常会受到遗传以及表观遗传不稳定性的影响,而且其最终并不会分化地太好,而这是正常的胚胎发育的关键,也是其融合到其它动物胚胎中的先决条件;事实上,在物种间转移的细胞中,仅有大约1%-3%的细胞能真正整合并促进发育。
为了提高细胞的数量,本文中,研究人员抑制了另外两种信号通路来产生原始的人类干细胞,其拥有稳定的基因组以及相对较少的基因调节故障,重要的是,其还具有完美的分化能力。此外,研究人员还使得一种有助于基因组稳定的重要基因发生突变,这不仅产生了有能力的干细胞,还产生了一种有竞争力的干细胞,其能更好地整合而并不会对宿主造成损伤;研究者Hanna说道,我们找到了一种新方法来让人类干细胞变得更有能力且更有竞争力,与此前我们所能做到的相比,干细胞成功转移的机会增加了大约5倍。

尽管此前研究结果表明,人类原始干细胞能分化为原始生殖细胞(卵细胞或精细胞的祖细胞),但本文研究中所产生的完全原始的干细胞也能分化为胚胎外组织、胎盘和卵黄囊细胞,从而维持发育中的胚胎,比如这种细胞能用作开发合成性胚胎的来源,而并不需要进行卵子的捐赠。利用小鼠干细胞来达到这种状态或许是特别难以完成的,而人类的细胞显然是不同的。这或许就是最令人惊讶的发现,其突出了人类和小鼠干细胞之间的差异,以及原始细胞的不同状态之间的差异,这些差异或许就表明,研究人员如果要使得开发定制化的器官成为现实,仍然还需要进行大量的工作。
研究者Hanna表示,理解这些差异或许对于克服干细胞研究和应用领域仍然面临的无数问题至关重要,比如,如果将来能在猪体内培育胰腺用于人体移植,我们就必须考虑不同物种之间大量的进化差异,首先就是人类和小鼠;而就目前而言,研究人员似乎朝着这一方向迈出了建设性的一小步。综上,本文研究为定义人类原始干细胞多能性的信号基础建立了一种重要的框架。


研究人员认为,使用鼻腔喷雾疫苗能在上呼吸道建立保护是减少SARS-CoV-2感染和传播的关键策略,对于最终控制COVID-19的大流行非常重要;综上,本文研究结果表明,以鼻腔内流感疫苗为基础的增强型疫苗或许能诱导机体粘膜和全身免疫力,从而就能在上呼吸道和下呼吸道有效预防SARS-CoV-2的感染和传播。
研究者Comert Kural教授说道,就好像我们的饮食习惯基本塑造了机体中的任何东西一样,细胞“吃”的方式对细胞的健康也至关重要;如今科学家们才明白这是如何发生的。文章中,研究者发现,一个细胞的细胞间机器或能组装成为一个高度弯曲的篮子样结构,最终生长成为一个封闭的笼子,此前科学家们认为这种结构开始时或许是一个平坦的晶格。膜的弯曲度很重要,其能控制将物质送入和带出的细胞“口袋”结构的形成,这些口袋结构能捕捉细胞周围的物质,并在细胞外物质周围形成,然后转变为囊泡结构(仅有红细胞大小的百万分之一),囊泡能将对细胞健康重要的物质(比如蛋白质)带入到细胞中,但其也能被感染细胞的病原体所劫持。
但这种口袋结构是如何从以前被认为是平坦形状的膜上所形成的,这个问题一直困扰了科学家们长达40年的时间,研究者Kural说道,这或许是细胞研究中的一个争议,而我们能使用超分辨率荧光成像技术来准确观察这些口袋结构是如何在活体细胞中形成的,因此我们也能够回答其是如何形成的等相关问题。简单来讲,与此前研究相比,研究人员制作了细胞的高分辨率“电影”而不是拍摄快照;实验研究结果显示,蛋白质支架一旦被招募到囊泡形成的位点,其就开始让底层膜变形了。

这或许与之前研究人员的假设形成了比对,即细胞的蛋白支架必须经过能量密集型的重组才能使得膜变弯曲。细胞消耗和排出囊泡的方式在生物体机体中扮演着非常关键的作用,这一过程有助于从血液中清除胆固醇,同时其还能传递神经信号,众所周知,这一过程在多种疾病中都会发生破坏,包括癌症和阿尔兹海默病等。Kural说道,理解膜结合囊泡的起源和动态学变化非常重要,其或能被用来运输药物以达到医学治疗的目的,但同时也会被诸如病毒等病原体劫持来进入并感染细胞;本文研究结果非常重要,不仅对于科学家们理解生命的基本原理,而且对于开发新型的治疗性策略至关重要。
组成人体的数万亿个细胞中的每一个每天都会遭受超过1万次DNA损伤,如果细胞无法修复的话这些损伤将会是灾难性的,但一种非常微妙的能检测和修复基因损伤的机器能够发挥作用来防止DNA突变以及诸如癌症等疾病的出现;在机器学习应用于高通量显微镜等技术的帮助下,研究人员就能设法详细观察这种DNA修复机器,并能识别出一种新的修复蛋白,相关研究结果以题为“Assessing kinetics and recruitment of DNA repair factors using high content screens”的形式发表在国际杂志Cell Reports上,或有望未来帮助科学家们开发新型癌症疗法。

在实验室中人体细胞的DNA被激光束破坏的图像
一旦出现DNA损伤,比如DNA双链断裂,细胞就会激活一种名为DNA损伤反应的机制,该机制就像“呼叫紧急服务”一样,这时候蛋白质就会快速与受损的DNA结合并发出警报信号,这就会被其它专门修复损伤的蛋白质所识别。化疗的目的是通过诱导DNA损伤来杀灭肿瘤细胞,其会促进癌症复发及死亡,通过了解DNA损伤发生以及其被修复的机制,研究人员就能了解到很多关于癌症如何发生以及如何去抵御它的相关知识,DNA修复方面的任何发现或许都将有助于开发新型癌症疗法,同时还能保护机体的健康细胞。
如今研究人员开发出了一种新方法,在研究者所开发的机器学习技术的帮助下就能对这一过程进行分析,其详细程度和精确度都是此前研究人员无法实现的,直到现在,追踪DNA修复动力学的一个限制性因素就是无法处理和分析显微镜所拍摄的图像所产生的大量数据。文章中,研究人员使用了高通量的显微镜,其能在诱导了细胞的遗传损伤后获得成千上万张细胞图片,在第一阶段,研究人员将300多张不同的蛋白质引入到细胞中,并在一次实验中评估其是否会随着时间的推移而干扰DNA的修复机制,该技术帮助研究人员发现了能参与DNA修复的9种新型蛋白。
但研究人员决定更进一步研究监测产生遗传损伤后的300种蛋白的功能,为了做到这一点,他们改编了一种经典的DNA微辐射技术(其能以紫外光来破坏DNA)首次在大规模的格式中使用,并分析了所研究的300种蛋白质的行为。研究者说道,我们观察到,许多蛋白质能吸附到损伤的DNA上,而其它蛋白质的表现则正好相反,其能远离DNA损伤,实际上其要么与受损的DNA结合,要么从受损的DNA上移开,从而就允许进行修复的蛋白被招募到损伤的病变部位,这是DNA修复蛋白的一个共同特征,而这两种现象都是相关的。
其中一个被发现的蛋白就是PHF20,这种蛋白质在损伤后的几秒内就会远离损伤部位并促进对DNA修复非常关键的53BP1蛋白的招募,没有PHF20蛋白的细胞无法合适地修复DNA,而且相比正常细胞而言其对辐射更为敏感,这就提示,PHF20蛋白对于DNA修复非常关键。

综上,本文研究结果表明,PHF20蛋白因子或能被排除在DNA断裂处,从而而通过与53BP1的招募竞争来影响DNA的修复过程,这些资源或许能被用于遗传扰动、小分子筛选和大规模的DNA修复分析,同时还能帮助理解和操控细胞中的DNA修复过程。
锻炼不仅能训练肌肉还能预防脂肪肝的发生;近日,一篇发表在国际杂志Molecular Metabolism上题为“Exercise prevents fatty liver by modifying the compensatory response of mitochondrial metabolism to excess substrate availability”的研究报告中,来自图宾根大学等机构的科学家们通过研究揭示了在机体锻炼的过程中会观察到哪些分子适应性,尤其是肝脏中线粒体的适应性。
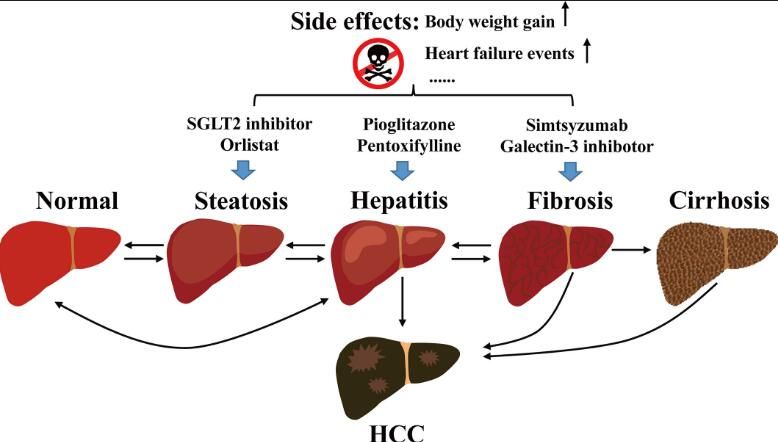

综上,本文研究提供了科学家们对肝脏和骨骼肌中的线粒体对高能量饮食和耐力训练的早期适应性进行了全面的分析,相关研究结果表明,锻炼或会使得高能量饮食诱导的来自丙酮酸的线粒体底物氧化水平的增加和乙酰辅酶A所驱动的脂质合成之间脱节,这或许有助于预防高脂肪和高糖类摄入对肝脏中线粒体功能和胰岛素敏感性的长期有害影响。
文章转载自生物谷,系出于传递更多信息之目的,转载内容不代表本站立场。如有侵权请及时联系,我们将立即进行删除处理。




 京公网安备 11011402010692号
京公网安备 11011402010692号




